上海曼博生物医药科技有限公司代理商
8 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.5999999999999996
- 0.5999999999999996
- 1.5999999999999996
- 0.5999999999999996
文献支持
PBS垂直轮生物反应器3L
¥1000000 - 3000000
代理商
上海曼博生物医药科技有限公司
入驻年限:8 年
- 联系人:
曼小博
- 所在地区:
上海 浦东新区
- 业务范围:
试剂、耗材、实验室仪器 / 设备、ELISA 试剂盒、抗体、技术服务、细胞库 / 细胞培养、书籍 / 软件
- 经营模式:
代理商
推荐产品
公司新闻/正文
RNAi 在靶点识别和验证中的应用_上海曼博生物
523 人阅读发布时间:2024-01-16 09:16
引言
基于功能丧失表型分析的基因筛选是靶点识别和验证的强大工具。 RNA 干扰 (RNAi) 仍然是该领域的一项成熟且有效的技术。 Horizon Discovery开发了基于 siRNA 的功能基因组筛选和验证平台。在这里,我们概述了我们的一项综合致死率研究,从初级筛选到deconvolution以及最终的靶标验证。
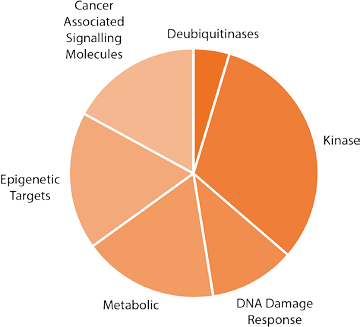
我们使用XMAN 同基因细胞系进行筛选,其中突变细胞系的不同之处仅在于癌症中经常发生突变的单个基因的改变。该系统为初步筛选提供了非常干净的基线,是一个很有价值的靶点发现模型系统。对于初步筛选,我们使用可成药基因组文库(druggable genome library),该文库针对约 2200 个肿瘤学中高度关注的基因(图 1)。
结果与讨论
初步筛选经多次优化,是在一对 Horizon discovery的同基因细胞系中进行的。所有的实验孔进行统一操作,与配对的野生型细胞系相比,通过检查突变基因型中经 siRNA 处理后细胞的相对活力来确定合成致死靶点基因(hits)。这个过程会产生一个综合的杀伤力分数,我们用它来对把靶点进行排名和分层。然后通过confirmation、deconvolution和validation对选定的靶标进行分类(见图 2)。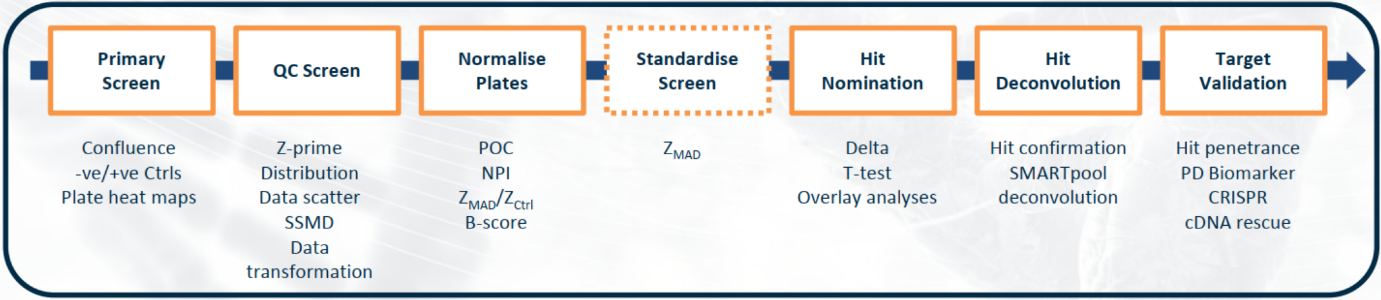
在这次筛选中,我们确定了许多有希望的合成致死候选物(图 3)。通过查询可用数据和文献,包括目标的成药潜力对靶点进行评估。然后进行靶点确认分析,这些分析包括在 2D 生长中解卷积和活力分析; mRNA 敲低的 RT-qPCR 分析;蛋白质敲低的蛋白质印迹分析;和 3D 增长中的生存能力分析。
在本应用中,我们仅以这些靶点中的一个基因的数据为例进行讨论。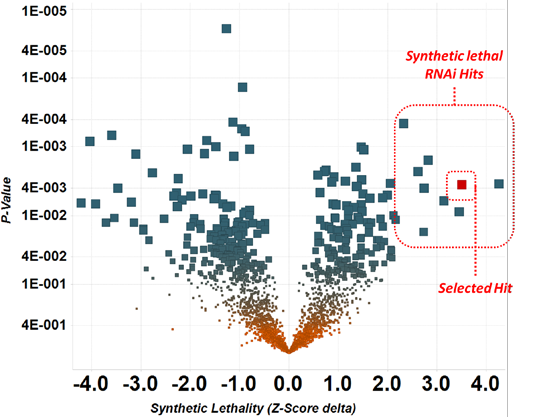
SMARTpool 的deconvolution实验结果显示,针对该靶点的单条siRNA试剂都对SMARTpool观察到的整体表型做出了贡献。
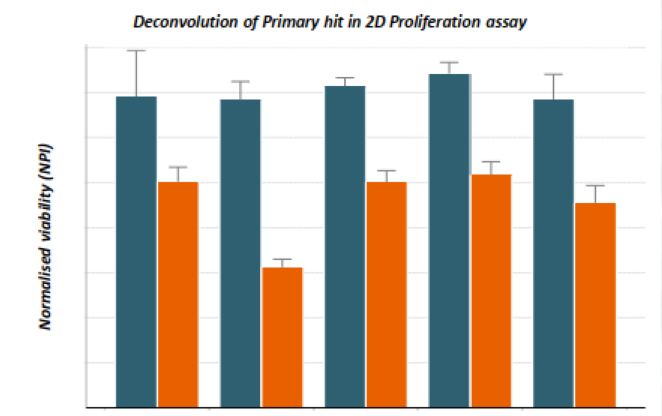
作为组合确认和验证分析的一部分,使用来自其他供应商和设计算法的siRNA产品来确认效果。然后使用同基因细胞系在 3D 细胞培养中进行表型评估。该测定使我们能够在更接近模拟体内细胞生长的条件下检查基因敲低(knockout)的表型效应。该测定可以深入了解与肿瘤中常见的代谢和氧梯度相关的治疗问题,也可以直接解决细胞-细胞和细胞-基质问题,这些相关问题的探究可能影响化学抗性机制的相互作用。
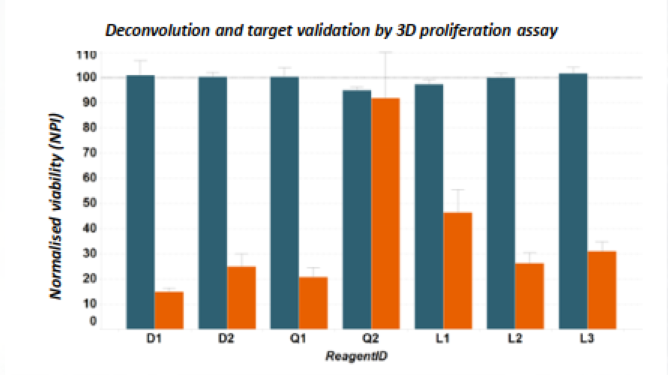
对于这个靶点基因,我们发现当细胞在3D培养条件测定中生长时,在 2D 生长培养中观察到的合成致死表型会加剧(图 5)。对于实验中使用的Q2 siRNA 试剂,在 3D 生长测定中未观察到显著的表型。当通过 RT-qPCR 分析该靶标的knockdown效应时,我们发现mRNA降低水平不明显(仅约 30% knockdown,图 6),与观察到的表型直接对应。
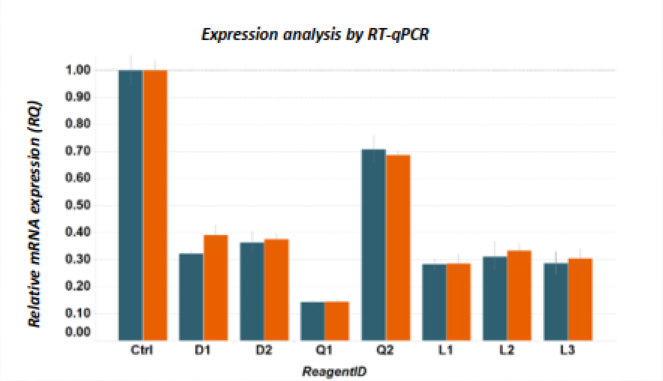
蛋白质的敲低水平(图 7)与 mRNA水平和观察到的表型效应密切相关。因此通过蛋白质印迹实验对蛋白表达水平进行评估。合成致死靶标的knockdown导致该生物标志物在亲本和突变细胞中显着一致丢失(图 7)。因此该靶点目标基因有希望继续进行深入研究。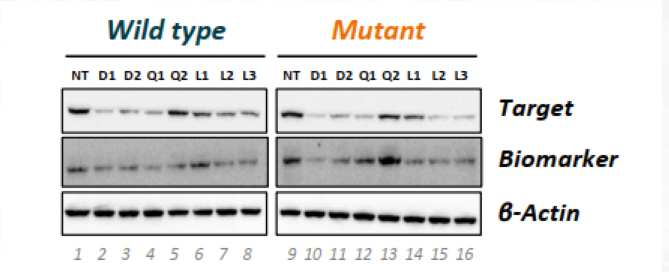
实验方法
二次筛选使用了 Dhamacon 单条 siGENOME 试剂、Qiagen Flexitube siRNA 试剂和 Ambion (LifeTech) Silencer Select siRNA 试剂。使用 Hoechst 染色或 AlamarBlue 试剂(LifeTech)监测增殖。 mRNA 的 RTqPCR 分析使用 LifeTech TaqMan 进行检测。
基于功能丧失表型分析的基因筛选是靶点识别和验证的强大工具。 RNA 干扰 (RNAi) 仍然是该领域的一项成熟且有效的技术。 Horizon Discovery开发了基于 siRNA 的功能基因组筛选和验证平台。在这里,我们概述了我们的一项综合致死率研究,从初级筛选到deconvolution以及最终的靶标验证。
我们使用XMAN 同基因细胞系进行筛选,其中突变细胞系的不同之处仅在于癌症中经常发生突变的单个基因的改变。该系统为初步筛选提供了非常干净的基线,是一个很有价值的靶点发现模型系统。对于初步筛选,我们使用可成药基因组文库(druggable genome library),该文库针对约 2200 个肿瘤学中高度关注的基因(图 1)。

图 1. Horizon Discovery 的可成药基因组 siRNA 文库的组成。该阵列文库使用 SMARTpools,可以靶向七大基因分类中的 2175 个基因。
结果与讨论
初步筛选经多次优化,是在一对 Horizon discovery的同基因细胞系中进行的。所有的实验孔进行统一操作,与配对的野生型细胞系相比,通过检查突变基因型中经 siRNA 处理后细胞的相对活力来确定合成致死靶点基因(hits)。这个过程会产生一个综合的杀伤力分数,我们用它来对把靶点进行排名和分层。然后通过confirmation、deconvolution和validation对选定的靶标进行分类(见图 2)。

图 2.常规的靶点筛选过程:从初次筛选到目标验证
在这次筛选中,我们确定了许多有希望的合成致死候选物(图 3)。通过查询可用数据和文献,包括目标的成药潜力对靶点进行评估。然后进行靶点确认分析,这些分析包括在 2D 生长中解卷积和活力分析; mRNA 敲低的 RT-qPCR 分析;蛋白质敲低的蛋白质印迹分析;和 3D 增长中的生存能力分析。
在本应用中,我们仅以这些靶点中的一个基因的数据为例进行讨论。

图 3. 初次筛选的数据和靶点识别情况。将每个靶点的 P 值与合成致死率的大小作图。
SMARTpool 的deconvolution实验结果显示,针对该靶点的单条siRNA试剂都对SMARTpool观察到的整体表型做出了贡献。

图 4. SMARTpool Regent 对应的单条siRNA 2D表型分析。亲本野生型细胞以蓝色显示,突变的同基因克隆以橙色显示。
作为组合确认和验证分析的一部分,使用来自其他供应商和设计算法的siRNA产品来确认效果。然后使用同基因细胞系在 3D 细胞培养中进行表型评估。该测定使我们能够在更接近模拟体内细胞生长的条件下检查基因敲低(knockout)的表型效应。该测定可以深入了解与肿瘤中常见的代谢和氧梯度相关的治疗问题,也可以直接解决细胞-细胞和细胞-基质问题,这些相关问题的探究可能影响化学抗性机制的相互作用。
对于这个靶点基因,我们发现当细胞在3D培养条件测定中生长时,在 2D 生长培养中观察到的合成致死表型会加剧(图 5)。对于实验中使用的Q2 siRNA 试剂,在 3D 生长测定中未观察到显著的表型。当通过 RT-qPCR 分析该靶标的knockdown效应时,我们发现mRNA降低水平不明显(仅约 30% knockdown,图 6),与观察到的表型直接对应。

图 5. 3D 表型分析。亲本野生型细胞以蓝色显示,突变的同基因克隆以橙色显示。

图 6. 使用 RT-qPCR 分析mRNA 表达水平以评估knockdown效应。亲本野生型细胞以蓝色显示,突变的同基因克隆以橙色显示
蛋白质的敲低水平(图 7)与 mRNA水平和观察到的表型效应密切相关。因此通过蛋白质印迹实验对蛋白表达水平进行评估。合成致死靶标的knockdown导致该生物标志物在亲本和突变细胞中显着一致丢失(图 7)。因此该靶点目标基因有希望继续进行深入研究。

图7. 靶标knockdown效应以及对应的生物标志物表达水平进行蛋白免疫印迹分析实验
实验方法
二次筛选使用了 Dhamacon 单条 siGENOME 试剂、Qiagen Flexitube siRNA 试剂和 Ambion (LifeTech) Silencer Select siRNA 试剂。使用 Hoechst 染色或 AlamarBlue 试剂(LifeTech)监测增殖。 mRNA 的 RTqPCR 分析使用 LifeTech TaqMan 进行检测。