上海曼博生物医药科技有限公司代理商
7 年
手机商铺
- NaN
- 0.40000000000000036
- 0.40000000000000036
- 1.4000000000000004
- 0.40000000000000036
上海曼博生物医药科技有限公司
入驻年限:7 年
- 联系人:
曼小博
- 所在地区:
上海 浦东新区
- 业务范围:
试剂、耗材、实验室仪器 / 设备、ELISA 试剂盒、抗体、技术服务、细胞库 / 细胞培养、书籍 / 软件
- 经营模式:
代理商
推荐产品
公司新闻/正文
CN Bio:一家经美国FDA验证过的微流控器官芯片系统供应商
226 人阅读发布时间:2025-08-15 11:07
近期,国家CDE发布《模型引导的罕见疾病药物研发技术指导原则》,将器官芯片正式列入非临床研究数据(详情可查看文末新闻)。过去十几年,CN Bio PhysioMimix微流控器官芯片系统一直经美国FDA验证,旨在共同推进器官芯片技术标准化与临床转化。
2012年
由美国FDA、NIH、DARPA牵头,CN Bio的微流控器官芯片PhysioMimix诞生于麻省理工学院,与哈佛大学之间开展了器官芯片技术竞赛。
2016年
CN Bio公司与麻省理工学院在这场竞赛中胜出,并于2018年开发出10器官芯片系统(发表于《自然·科学报告》[1])。
2017年
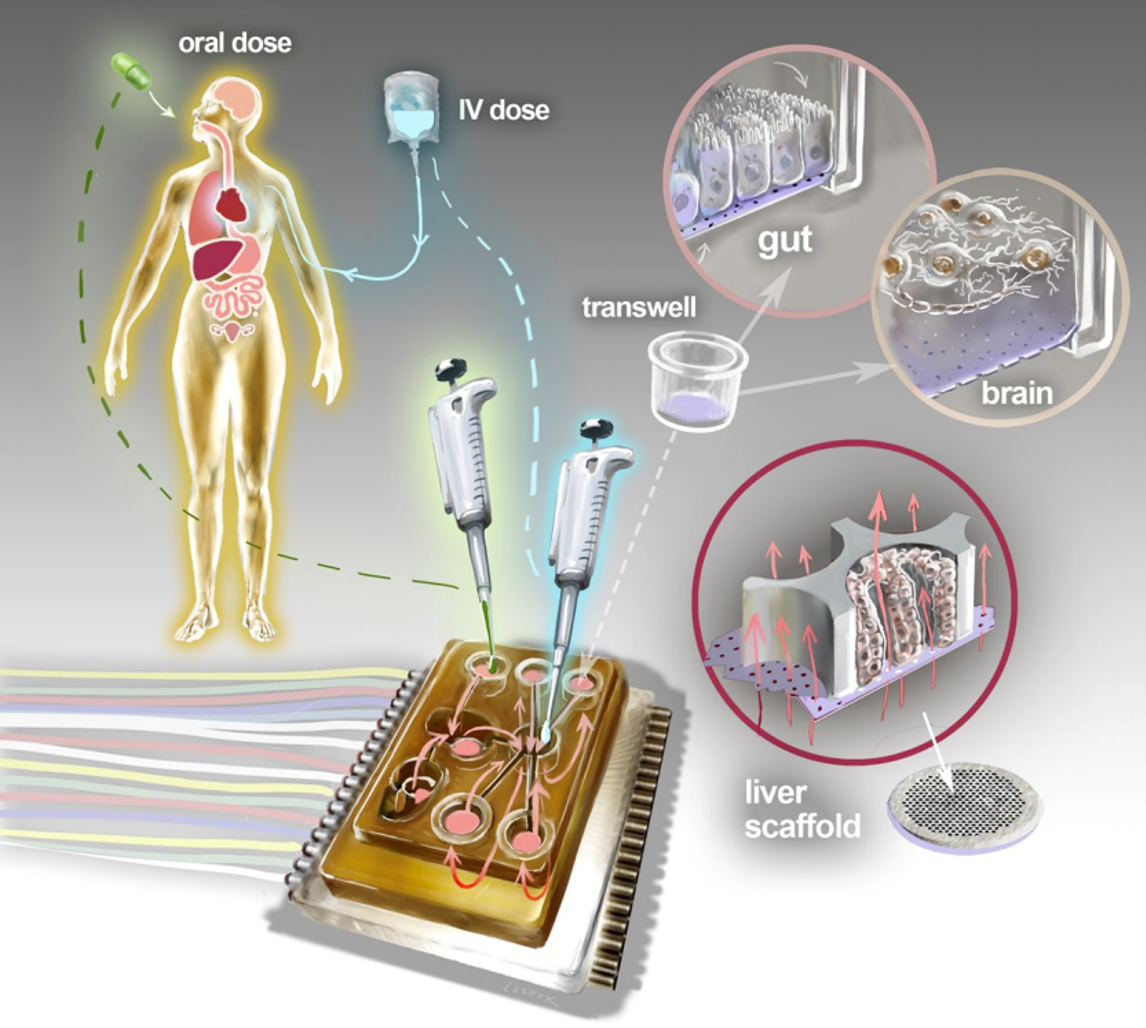
FDA的药物评价与研究中心(CDER)与CN Bio合作,并于2020年共同发表第一篇关于肝脏微生理系统(MPS)在安全性/药理学应用中的特性研究[2],待测药物与体内结果一致,证明器官芯片用于药物分布、积累、代谢、毒性方面的潜力。

FDA(CDER)与CN Bio合作,共同发表第一篇肝脏微生理系统(MPS)的评估文章
2022年
FDA在CN Bio Innovations 肝芯片中表征不同批次的人原代肝细胞,给用户使用器官芯片如何独立预验证细胞提供了指南。
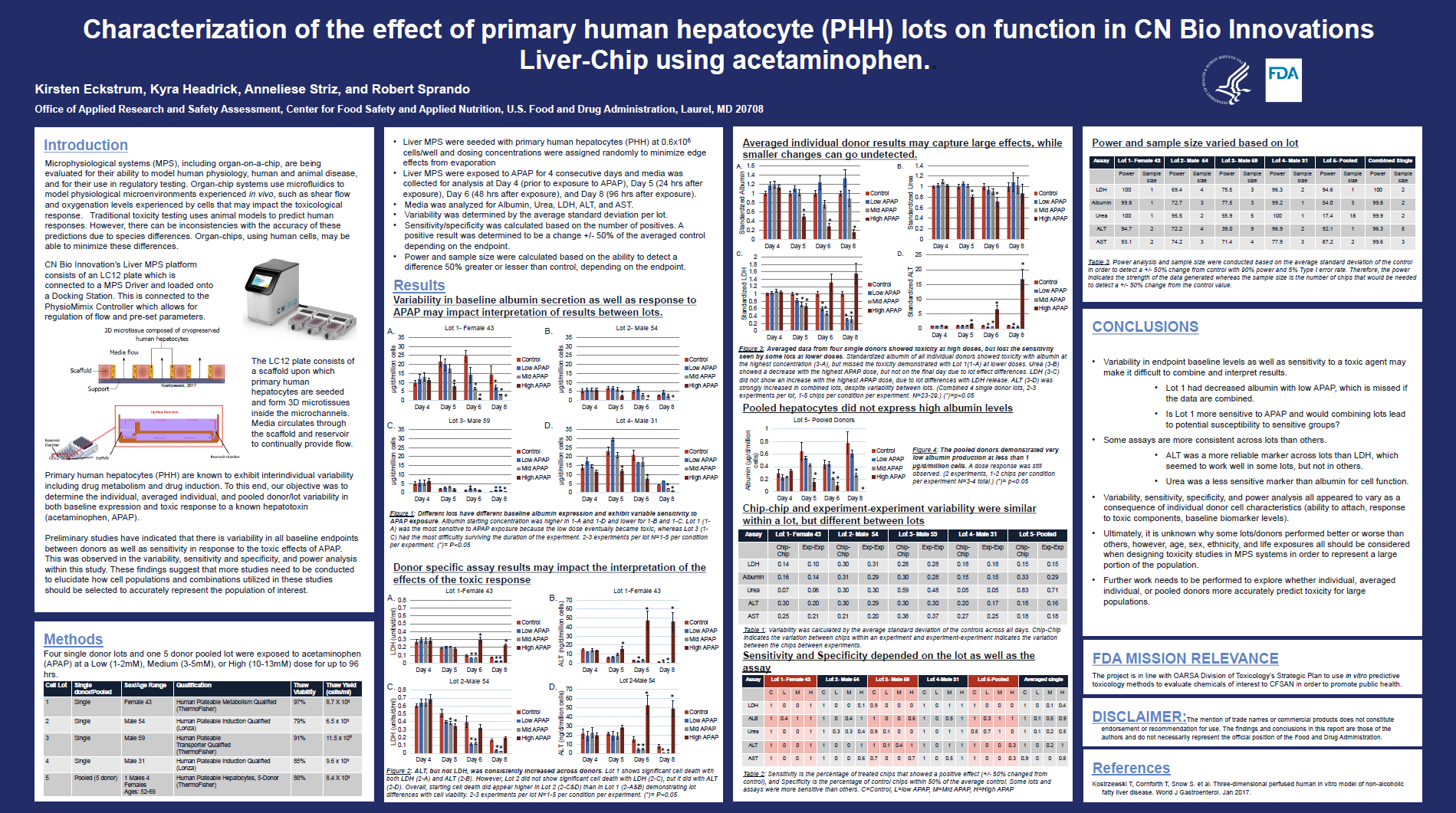
FDA在CN Bio肝芯片中表征不同批次的人原代肝细胞
2023年
FDA通过了Inipharm的INI-822(与代谢性肝病有关)进入临床试验阶段,该小分子的有效性数据依靠CN Bio产生,是器官芯片供应商提供数据支持肝病药物进入临床的第一个例子[3]。
CN Bio PhysioMimix数据支持Inipharm的INI-822用于治疗代谢性肝病,获FDA审批通过进入IND
2024年
FDA继续评估CN Bio的肺芯片,该研究的数据/结果可用于制定MPS的性能标准和质量控制标准草案指南的制定。
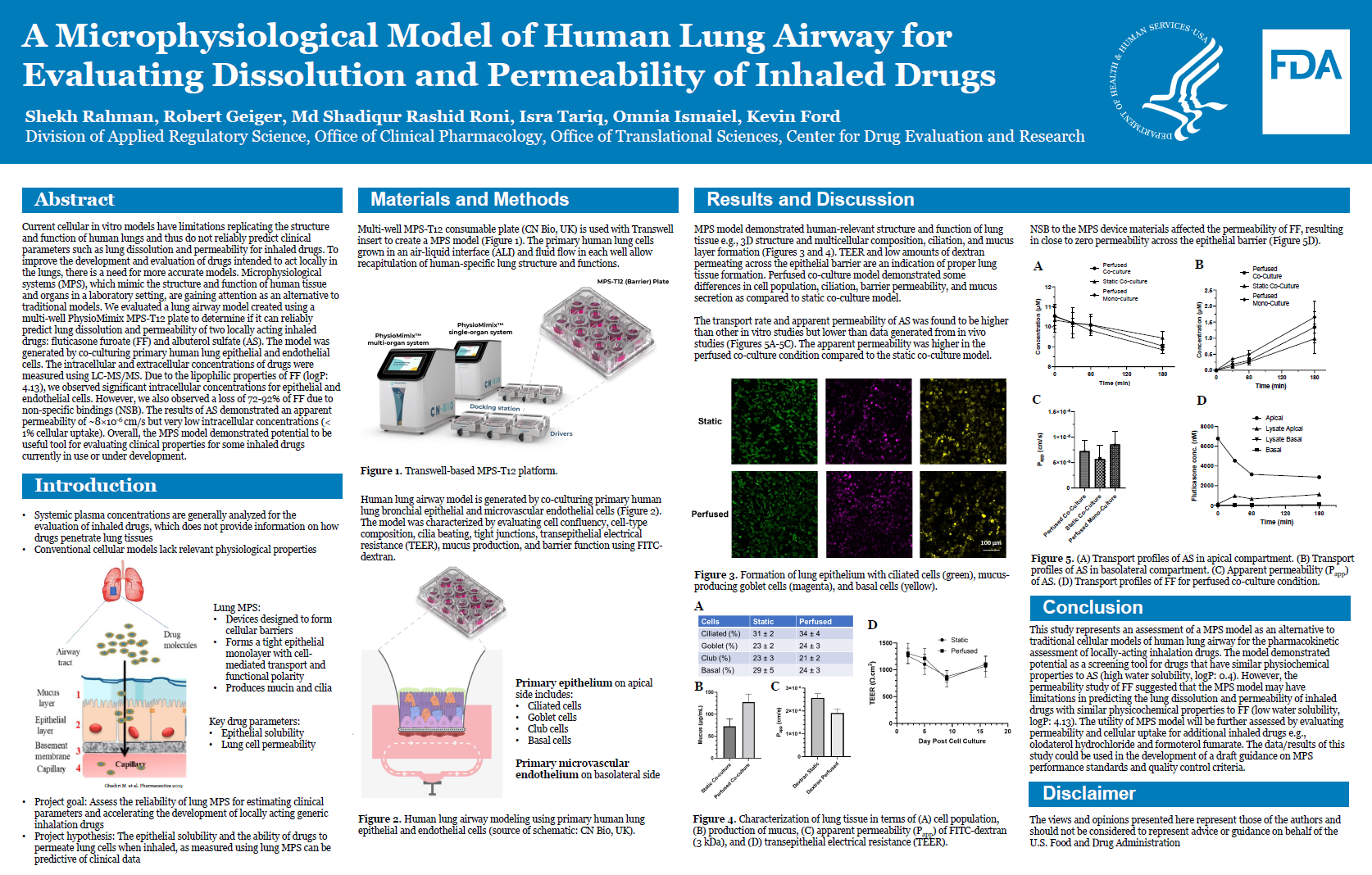
FDA评估CN Bio的肺模型
2025年
FDA宣布逐步取消单抗类药物动物试验要求,承认新兴技术(如类器官、器官芯片、计算机建模等)可能比传统动物试验更能预测人体反应[4]。7月初,CN Bio 参与由 3Rs 协作组织牵头、与 FDA 合作的项目,旨在增强肝类微生理系统(Liver MPS)在药物性肝损伤(DILI)研究中的可信度[5]。
CN Bio参与由3Rs协作组织牵头,与FDA合作的器官芯片项目
中国器官芯片行业开拓者发展理念
作为中国器官芯片领域的专业服务者与资源整合方,曼博生物专注于连接国际前沿技术与本土产业需求,致力于弥补国内器官芯片行业在技术标准化与产业链协同中的短板。通过引入经全球权威机构验证且应用互补的器官芯片技术(CN Bio就是其中之一),我们提供从技术适配、产品供应到场景化应用支持的综合服务,助力中国生物医药企业、科研机构及相关单位探索更优质、更符合伦理的药物研发路径,逐步推动器官芯片在药物开发、有效性评估、毒性评估等领域的实践应用。
近期新闻
2025年7月30日,国家药品监督管理局药品审评中心(CDE)正式发布《模型引导的罕见疾病药物研发技术指导原则》(以下简称《指导原则》)[6],该文件为2024年10月发布的《模型引导的罕见病药物研发技术指导原则(征求意见稿)》的正式实施文件。
该《指导原则》明确将器官芯片技术列为支持罕见病药物研发的关键技术工具,表明Regulatory authorities对该项技术的进一步支持,助力推动我国罕见病药物研发领域的规范化与提效进程。