上海曼博生物医药科技有限公司代理商
8 年
手机商铺
- NaN
- 0.5999999999999996
- 0.5999999999999996
- 1.5999999999999996
- 0.5999999999999996
上海曼博生物医药科技有限公司
入驻年限:8 年
- 联系人:
曼小博
- 所在地区:
上海 浦东新区
- 业务范围:
试剂、耗材、实验室仪器 / 设备、ELISA 试剂盒、抗体、技术服务、细胞库 / 细胞培养、书籍 / 软件
- 经营模式:
代理商
推荐产品
公司新闻/正文
器官芯片整体解决方案(一):肿瘤(类器官)芯片及肝脏芯片的3大应用_曼博生物
764 人阅读发布时间:2025-01-08 10:28
在药物开发、疾病研究和毒理学测试等领域,传统的动物模型和二维细胞培养常常无法再现人体内的复杂生理环境。这不仅导致了药物研发效率低下,还增加了高风险的失败率。面对这一挑战,器官芯片技术正逐渐成为解决方案,为现代医学带来进一步的突破。
上海曼博生物一直关注3D培养、类器官及器官芯片领域的前沿发展,致力于为客户提供解决方案。上期我们已为大家带来了“3D培养/类器官”的整体解决方案(可点击查看)。
本期我们将为大家介绍肿瘤(类器官)芯片及肝脏芯片的3大应用,帮助科学家提升药物研发效率、优化毒理学测试,并推动疾病模型研究的深入发展。
概述:基于器官芯片培养各种组织/器官的应用
器官芯片目前主要有两个大的潜在方向:药物研发和个体化治疗。其中,药物研发领域会是器官芯片应用的第一轮,该领域还包括化学物质、食品、化妆品的研发。器官芯片的应用贯穿药物开发全流程,包括但不限于疾病建模、安全性毒理学、ADME /药理学。
我们将分别从肿瘤(类器官)芯片、肝脏芯片、肠道芯片、肺芯片、血脑屏障芯片、神经芯片、皮肤芯片和其他器官芯片展开介绍,如果您对类器官感兴趣,可点击查看类器官相关内容。
1、肿瘤(类器官)芯片(PDTOs-on-chip)
肿瘤通常由高度异质的细胞群组成,这导致其对化疗的反应存在差异。使用传统的2D培养肿瘤细胞系往往不能正确反映药物在体内的耐药情况。有研究者(下图)使用基于微流控的高通量器官芯片板(推荐品牌:AKITA)来培养患者来源的肿瘤类器官(可点击查看) (Patient-Derived Tumor Organoids,PDTOs),在液流的不断灌注下,肿瘤组织显示出比2D静态培养条件下对化疗药物更顽强的抵抗能力,甚至可以在液流中加入免疫细胞来检测治疗效果。
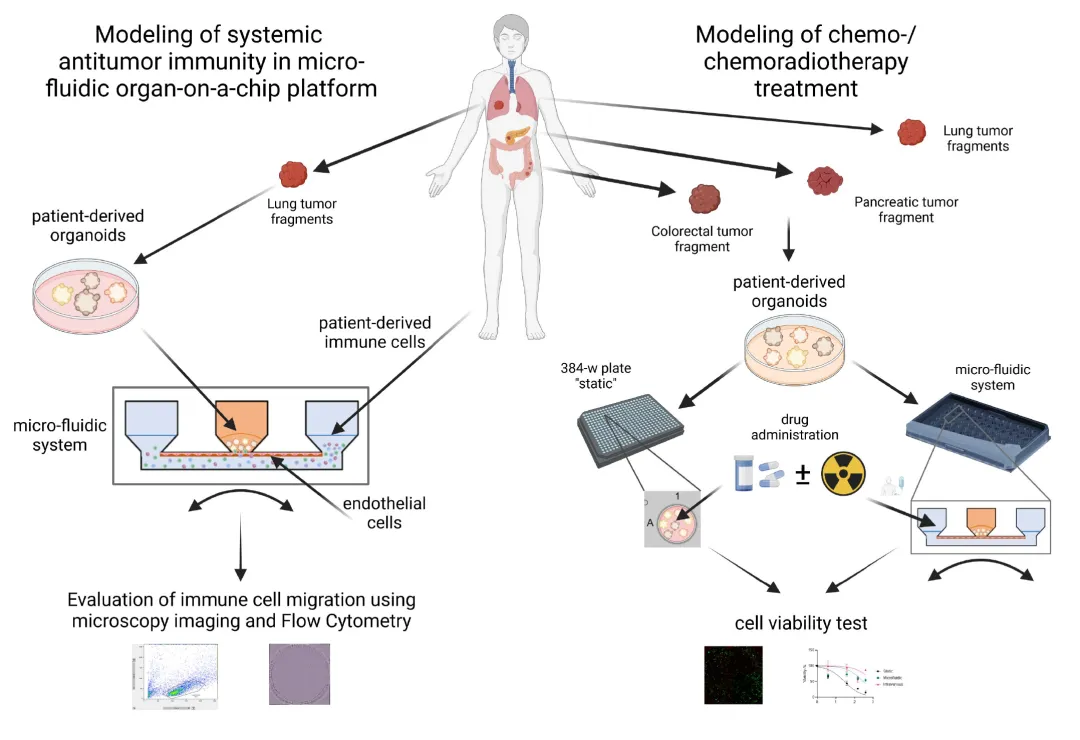
图:AKITA用于测试静脉注射药物和免疫细胞输送的肿瘤芯片模型
除了小分子药物外,器官芯片也可以兼容免疫疗法、腺病毒、溶瘤腺病毒等新治疗模式(可点击查看)(下图),这是传统的2D静态培养所达不到的效果。
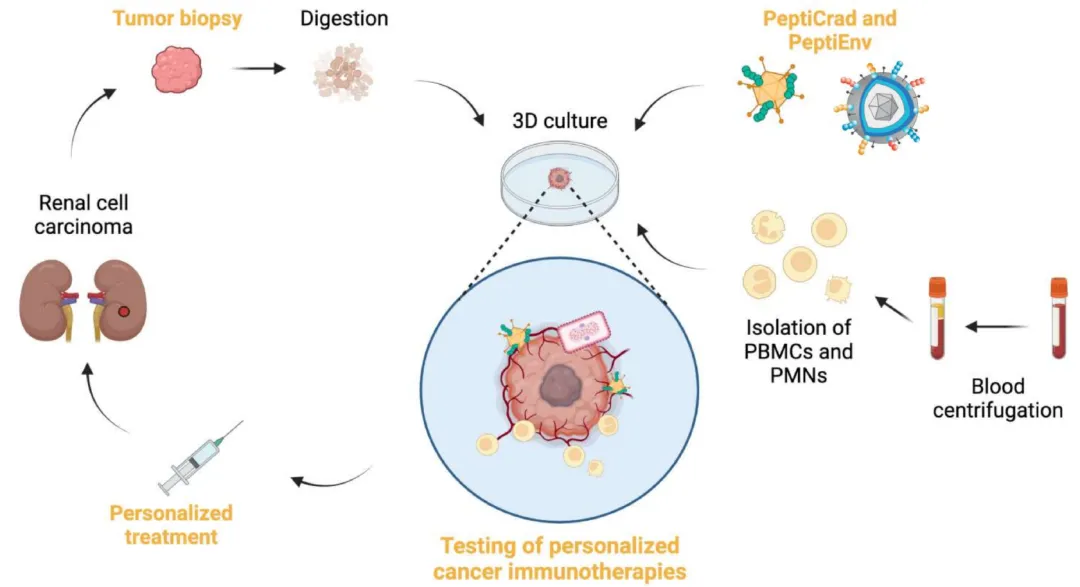
图:基于微流体器官芯片3D培养的肿瘤免疫疗法或腺病毒、溶瘤腺病毒模式图
建立能够再现患者肿瘤和免疫系统的改进型临床前人类模型,将为测试患者特异性反应、开发个性化治疗方案铺平道路,并加速其进入临床的进程。
2、肝脏芯片(Liver-on-chip)
肝脏一直是药物开发关注的重点,而基于微流控器官芯片所构建的体外肝模型相较于传统静态培养原代肝细胞,则展现出更好的生理相关性。
应用一:毒性研究
肝脏是最易受药物毒性和药物性肝损伤(DILI)影响的器官之一。DILI是药物消耗的主要原因,已知超过750种FDA批准的药物具有一定程度的DILI风险,当前技术的局限性主要有:体外到体内翻译效果不佳;未能对毒性原因提供深入的机制见解;许多先进的体外模型的通量较低,限制了数据点的数量;进行慢性暴露试验具有挑战性;不可能产生有毒的 I 期和 II 期代谢物等,此外,由于遗传或免疫反应差异,细胞系/动物模型不太适合测试新的人类特异性模式(可点击查看)。
器官芯片能够灌注下以 3D 形式培养的人类原代肝实质细胞和非实质细胞(NPC),以形成组织,从中可以检测功能性肝脏特异性终点,这项技术可以利用临床生物标志物报告将实验室数据翻译、转化为临床数据,评估多个细胞终点以确定毒性机制,生成每个3D组织中多种化合物的完整剂量反应曲线,长期肝培养可促进数周的重复给药,将毒性 I 期和 II 期代谢物的产生与细胞健康测量关联起来。
该项技术被称为器官芯片(OOC)或微生理系统(MPS),代表性供应商之一是英国的 CN Bio ,旗下的PhysioMimix被FDA深度评价(可点击查看),在药物开发的监管机构认可度层面非常权威。
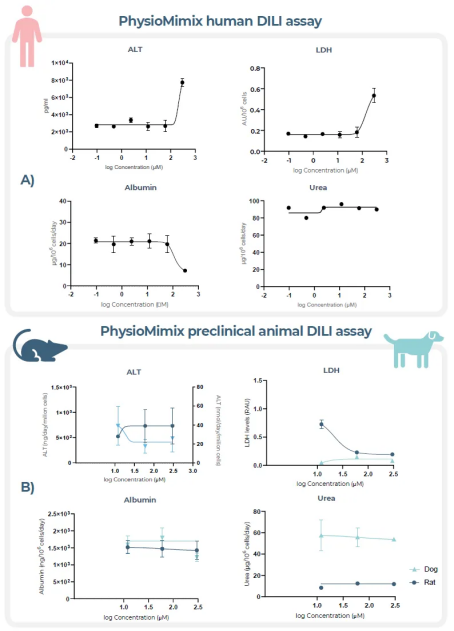
图:人类DILI OOC/MPS模型检测西他生坦sitaxentan的毒性数据与临床一致,而动物模型并未检测出DILI
另外,来自Charles River的研究团队将CN-Bio的肝脏芯片(Liver-on-Chip,LOC)技术应用于遗传毒性(可点击查看)测试产生了更有预测性的人体结果,潜在地有助于弥补体外和体内研究之间的差距(下图)。
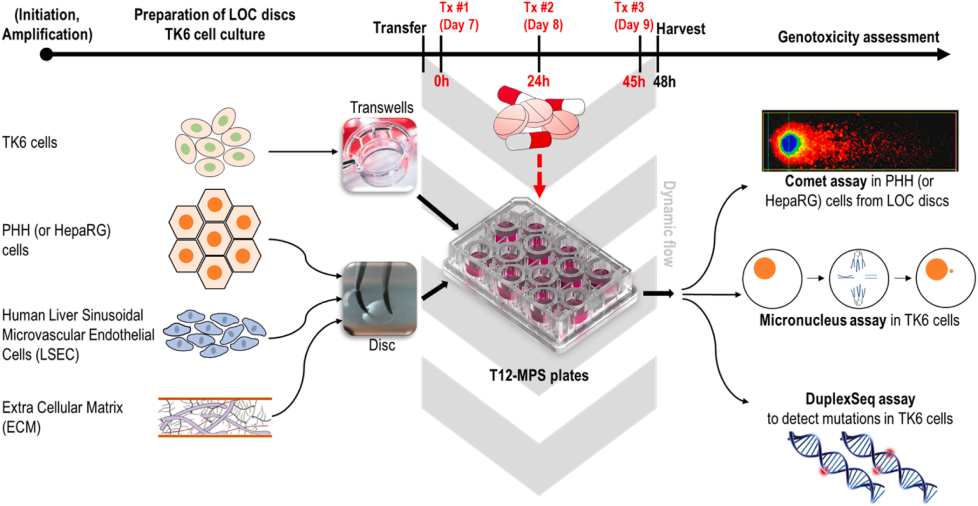
图:用于遗传毒性测试的芯片肝脏(LOC)模型概述
非酒精性脂肪肝病 (NAFLD) 是全世界导致慢性肝脏疾病的最常见的原因之一。在西方,它影响了约20-30%的成年人。大约有20%的被诊断为NAFLD的人继续发展为 非酒精性脂肪性肝炎(NASH)(可点击查看), 伴随着脂肪变性、炎症、肝脏中免疫细胞的出现和胰岛素抵抗相关。目前的临床前模型无法复制人类 NASH,这是导致药物流失的一个因素。
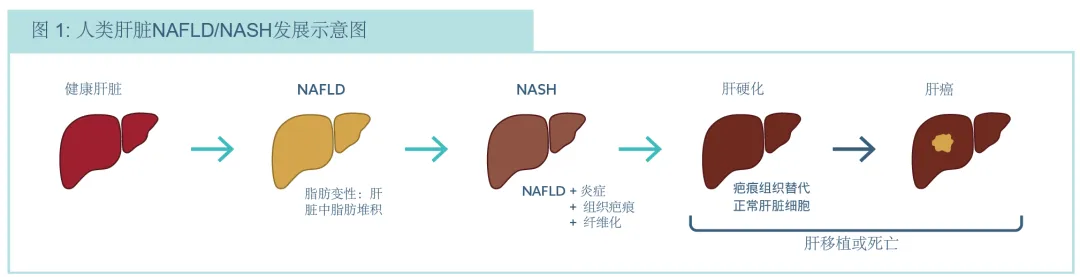
图:人类肝脏NAFLD/NASH发展示意图
器官芯片NASH 模型,使用三种人肝主要细胞,在高脂培养基的持续14天的灌注下(下图),其全转录谱,相比于小鼠模型,与人类样本匹配度更高,对NASH治疗药物作用效果的测试,从可溶性炎症和纤维化生物标志物定量、免疫荧光染色和共聚焦成像等方面,结果也更加准确。目前,已经有NASH器官芯片的数据支持药企(Inipharm的INI-822用于代谢性肝病治疗)经过FDA的检验(可点击查看),通过IND申报,目前正在进行临床测试。
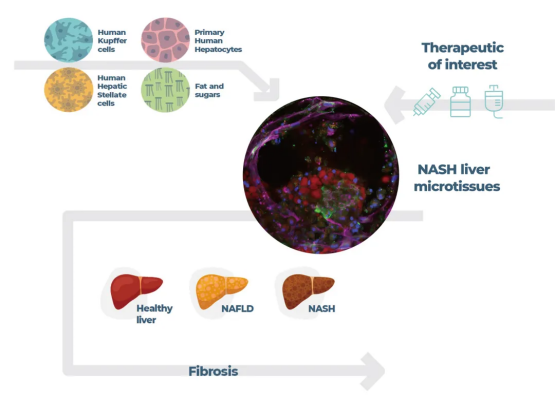
图:使用肝芯片模型产生类似NASH的表型
乙型肝炎病毒(HBV)感染与肝硬化和肝癌的发展密切相关,但目前能治愈乙肝的药物很少,主要是在药物研发过程中,由于缺乏合适的体外模型来概括肝细胞中病毒生命周期的所有步骤,以及难以为HBV复制建立生理上完整的宿主细胞模型。肝细胞是 HBV 的靶细胞,由于肝脏是一个复杂的 3D 结构,即使有原代肝细胞(PHH)作为疾病模型静态培养,但它们也会在培养过程中快速去分化(形态改变、CYP450酶活性丧失等)。
器官芯片能构建剖析HBV的全生命周期(可点击查看),包括患者源HBV的复制和HBV的cccDNA,可以维持肝功能至少40天。研究发现,感染HBV后的先天免疫和细胞因子反应与在HBV感染患者中观察到的反应相似,因此可以分离对免疫逃避和生物标志物验证重要的途径。
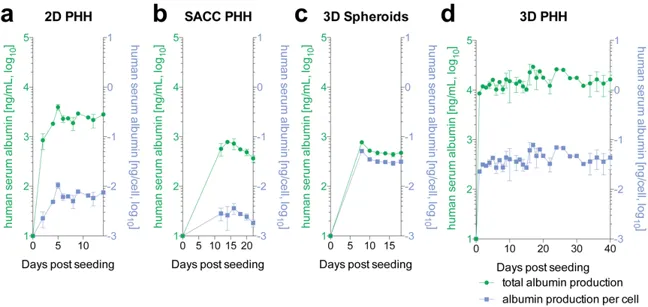
图:不同肝细胞培养模型的纵向白蛋白分泌
吸收(Absorption)、分布(Distribution)、代谢(Metabolism)和排泄(Excretion),即ADME是指示药物给药后行为的四个关键过程,在表征化合物的药代动力学(PK)性质和生物利用度方面起关键作用。口服生物利用度是指药物在通过肠壁吸收和肝脏首过代谢后到达全身循环的比例。ADME和生物利用度在确定化合物的安全性和毒理学特征方面至关重要,因此是药物开发前临床阶段的重要测量指标。
在一项对184种化合物的开创性研究中,发现动物模型与人类生物利用度的相关性较弱(R² = 0.34),而简单的肠道(如Caco-2细胞系)或肝脏(如肝微粒体和悬浮肝细胞)模型要么无法解释肝脏代谢,要么无法顾及肠道吸收。
器官芯片能使多个器官(如肠-肝、肺-肝)通过液流连接在一起,以模拟药物吸收和首过代谢等过程(可点击查看)(下图)。
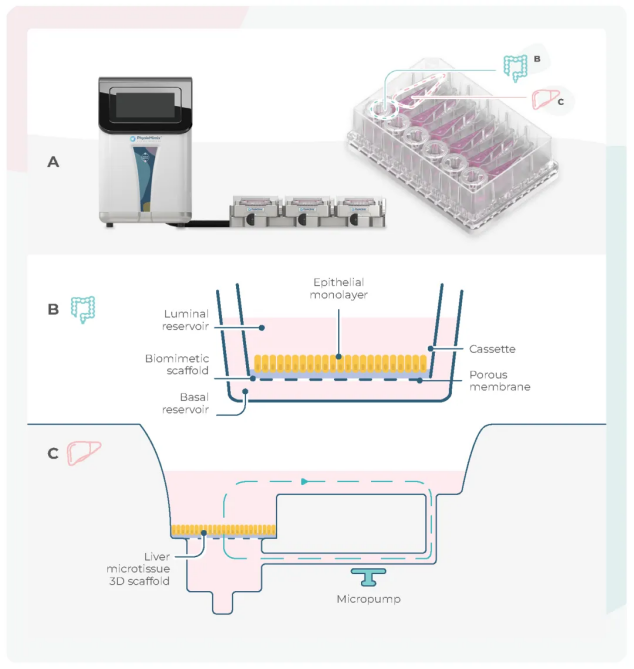
图:在双器官芯片中,肠-肝的设置
已有的数据表明,多器官组成的器官芯片,其人体药物生物利用度数据的相关性会高于其他模型(下图),在这一块的应用,罗氏(可点击查看)最近的发表的研究十分有说服力。
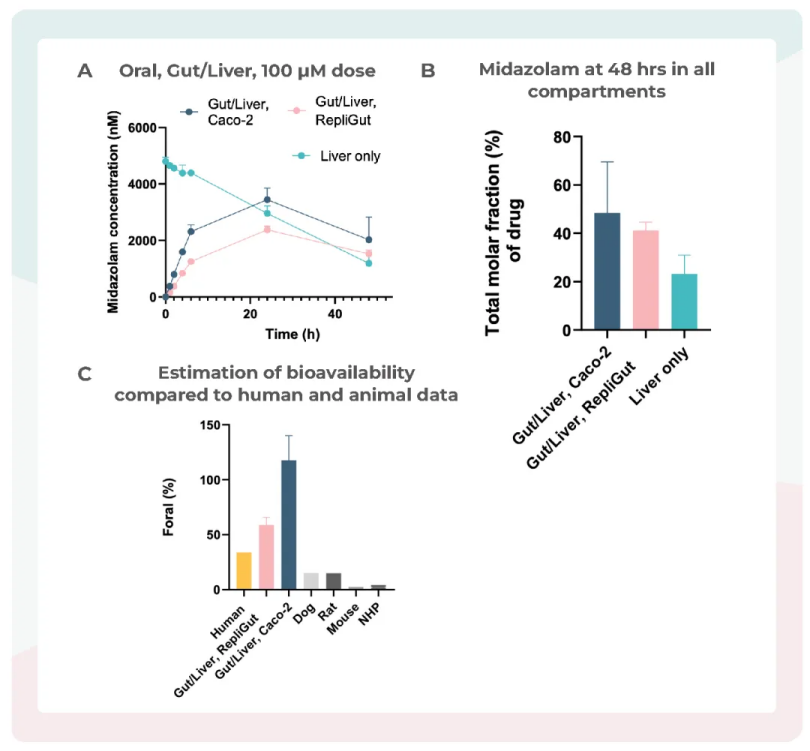
图:肠-肝器官芯片改善Midazolam人类生物利用度的相关性
以上是对肿瘤(类器官)芯片及肝脏芯片的整体解决方案,下期我们将为大家带来肠道芯片及肺芯片的方案,如果您有器官芯片的构建、应用、技术相关的疑问,欢迎联系我们,也欢迎关注“曼博生物”公众号,发送关键词“器官芯片”的获取相关资源。